A eficácia dos antibióticos na peri-implantite: Há padronização e biomarcadores de respostas? Uma revisão sistemática
THE EFFICACY OF ANTIBIOTICS IN PERI-IMPLANTITIS: ARE THERE STANDARDIZATION AND BIOMARKERS OF RESPONSES? A SYSTEMATIC REVIEW
LA EFICACIA DE LOS ANTIBIÓTICOS EN LA PERIIMPLANTITIS: ¿EXISTEN ESTANDARIZACIÓN Y BIOMARCADORES DE RESPUESTA? UNA REVISIÓN SISTEMÁTICA
Autor
URL do Artigo
https://iiscientific.com/artigos/1332EA
DOI
doi.org/10.63391/1332EA
Resumo
Summary
Resumen
INTRODUÇÃO
A peri-implantite é uma inflamação crônica dos tecidos ao redor de implantes dentários, levando à perda óssea. Diferente da mucosite, ela envolve destruição óssea devido a biofilme e resposta imunoinflamatória. Diversos fatores contribuem para seu desenvolvimento, como má higiene, tabagismo, histórico de periodontite, doenças sistêmicas (diabetes, dislipidemias) e predisposição genética, que afetam o microbioma e a resposta inflamatória, influenciando a severidade da doença e sua correlação com a inflamação sistêmica. (Blanco et al., 2021; Herrera et al., 2023).
O tratamento ainda carece de consenso, com abordagens que vão da descontaminação mecânica a cirurgias regenerativas, e o uso de antibióticos como adjuvantes, cuja eficácia varia. A falta de padronização nos protocolos clínicos e a heterogeneidade da literatura dificultam a escolha de tratamentos eficazes, evidenciando a necessidade de revisões sistemáticas e guias baseados em evidências. (Herrera et al., 2023; (Al-Khureif et al., 2020).
Biomarcadores inflamatórios e regenerativos em fluidos orais surgem como uma alternativa promissora para diagnóstico, monitoramento e personalização do tratamento, embora a padronização de métodos e valores de referência ainda seja um desafio. A abordagem personalizada, integrando dados clínicos e moleculares, pode otimizar a escolha terapêutica e a previsibilidade dos resultados, mas ainda há lacunas na literatura quanto à efetividade de antibióticos e validação de biomarcadores para uso rotineiro. (Hentenaar et al., 2021; Rakic et al., 2020; Herrera et al., 2023).
Justifica-se, portanto, a realização de uma revisão sistemática que investigue, de forma abrangente, a eficácia dos antibióticos na peri-implantite, considerando também a existência de protocolos padronizados e a aplicação de biomarcadores como parâmetros terapêuticos. A ausência de diretrizes consensuais e a carência de dados robustos que integrem aspectos microbiológicos, clínicos e moleculares constituem a problemática central deste estudo. Com o aumento da demanda por tratamentos implantossuportados e a crescente preocupação com falhas terapêuticas, torna-se essencial estabelecer bases científicas mais sólidas que orientem a prática profissional (Blanco et al., 2021; Gul et al., 2020; Herrera et al., 2023).
Dessa forma, o presente estudo tem como objetivo geral analisar a eficácia dos antibióticos no tratamento da peri-implantite, investigando a existência de protocolos padronizados e a utilização de biomarcadores na avaliação da resposta terapêutica. Como objetivos específicos, propõe-se: (1) avaliar os diferentes esquemas antibióticos utilizados no tratamento da peri-implantite e sua eficácia clínica e microbiológica; (2) investigar a existência de padronização nos protocolos terapêuticos envolvendo antibióticos em casos de peri-implantite; e (3) identificar e analisar os principais biomarcadores utilizados na monitorização da resposta inflamatória e da regeneração óssea em pacientes com peri-implantite tratados com antibióticos.
REFERENCIAL TEÓRICO
ETIOLOGIA E MECANISMOS PATOGÊNICOS DA PERI-IMPLANTITE
A peri-implantite é uma condição inflamatória que se instala a partir de alterações microbianas específicas na microbiota peri-implantar, comumente resultantes do acúmulo de biofilme bacteriano e da resposta imunológica inadequada do hospedeiro. O processo inflamatório leva à destruição progressiva do osso ao redor do implante, sendo essa perda influenciada pela virulência dos patógenos, pela ausência de barreiras anatômicas periodontais naturais e pela suscetibilidade individual do paciente (Rokaya et al., 2020).
Um dos fatores mais evidentes no desencadeamento da peri-implantite é a disbiose microbiana, caracterizada por um desequilíbrio ecológico entre microrganismos comensais e patógenos. Em comparação com a periodontite, a microbiota da peri-implantite apresenta maior diversidade, com predomínio de bactérias gram-negativas anaeróbias, como Porphyromonas gingivalis, Tannerella forsythia e Treponema denticola. A desorganização dessa microbiota leva à ativação exacerbada de receptores de reconhecimento padrão e à liberação de citocinas pró-inflamatórias, promovendo o dano tecidual (Cui et al., 2025).
A resposta imune ao biofilme peri-implantar é mediada por células inflamatórias que liberam interleucinas, metaloproteinases e espécies reativas de oxigênio, intensificando o processo destrutivo. Além disso, o sistema imunológico do hospedeiro pode apresentar falhas de regulação, o que agrava a inflamação e favorece a progressão da doença. Fatores como polimorfismos genéticos e variações epigenéticas também podem interferir na modulação da resposta imunológica frente aos patógenos (Atieh et al., 2020).
Condições sistêmicas, como diabetes mellitus e obesidade, alteram significativamente a resposta inflamatória ao redor dos implantes, tornando o ambiente mais propenso à instalação e progressão da peri-implantite. O aumento de citocinas inflamatórias circulantes e a resistência à insulina, frequentemente observados nesses pacientes, resultam em menor capacidade de reparo tecidual e em maior destruição óssea peri-implantar (Gasmi Benahmed et al., 2022).
Outros fatores locais e sistêmicos atuam como coadjuvantes na etiopatogenia da peri-implantite. O tabagismo, por exemplo, reduz o fluxo sanguíneo nos tecidos moles, prejudica a função de neutrófilos e altera o microbioma peri-implantar, contribuindo para a destruição óssea. Já o excesso de carga oclusal sobre implantes também tem sido associado a inflamação e falhas na osseointegração, mesmo na ausência de biofilme evidente, destacando a multifatorialidade da doença (Rokaya et al., 2020).
A ausência de ligamento periodontal e a menor vascularização ao redor dos implantes comprometem a defesa imunológica local e tornam os tecidos peri-implantares mais vulneráveis à colonização bacteriana e à inflamação crônica. Além disso, a topografia da superfície do implante e a morfologia das próteses podem favorecer o acúmulo de biofilme, dificultando sua remoção mecânica e favorecendo a recidiva da infecção (Atieh et al., 2020).
A combinação de fatores predisponentes e determinantes, como higiene oral deficiente, história de doença periodontal, uso prolongado de medicamentos imunossupressores e características anatômicas locais, exige uma abordagem clínica integrada e personalizada. A etiologia da peri-implantite, portanto, envolve um conjunto complexo de elementos que interagem dinamicamente ao longo do tempo e que, se não identificados e controlados precocemente, levam à falência do implante (Atieh et al., 2020; Rokaya et al., 2020).
ABORDAGENS ANTIMICROBIANAS NO TRATAMENTO DA PERI-IMPLANTITE: EFICÁCIA DOS ANTIBIÓTICOS
O tratamento da peri-implantite tem sido alvo de inúmeras estratégias terapêuticas com o objetivo de controlar a infecção, interromper a destruição óssea e promover a estabilidade clínica dos implantes. Entre essas estratégias, o uso de antibióticos, tanto por via local quanto sistêmica, tem sido amplamente discutido na literatura científica. Os antibióticos são utilizados como coadjuvantes às terapias mecânicas e cirúrgicas, visando à eliminação de patógenos e à modulação da resposta inflamatória local (Herrera et al., 2023).
A utilização de antibióticos sistêmicos apresenta vantagens em casos de infecção extensa ou quando o acesso mecânico é limitado. Contudo, sua eficácia depende de fatores como a penetração tecidual, a adesão ao regime terapêutico e a sensibilidade dos microrganismos envolvidos. Além disso, há controvérsias quanto à real contribuição dos antibióticos sistêmicos para o controle clínico da peri-implantite, especialmente em função da crescente resistência bacteriana e da ausência de padronização nos protocolos utilizados (Rokaya et al., 2020).
Por outro lado, os antibióticos de aplicação local têm sido empregados para obter concentrações elevadas do fármaco diretamente na região afetada, minimizando os efeitos sistêmicos e o risco de resistência. Esses agentes podem ser aplicados sob forma de géis, fibras ou chips contendo substâncias como clorexidina, minociclina e doxiciclina. Apesar dos resultados promissores em curto prazo, estudos indicam que a resposta clínica pode ser variável, e a manutenção dos efeitos depende de intervenções periódicas e de adequada higiene oral por parte do paciente (González Regueiro et al., 2021).
Outro ponto relevante é a escolha do tipo de antibiótico, que deve considerar o espectro de ação e a presença de microrganismos resistentes. Antibióticos como amoxicilina, metronidazol, azitromicina e doxiciclina são os mais utilizados, sendo frequentemente prescritos em associação para ampliar o espectro de cobertura. No entanto, a definição de esquemas terapêuticos eficazes ainda é um desafio, especialmente diante da variabilidade microbiológica e da falta de critérios clínicos uniformes para indicação da terapia antibiótica (Herrera et al., 2023).
A decisão pelo uso de antibióticos deve considerar não apenas a extensão da infecção, mas também aspectos como a presença de comorbidades, histórico de periodontite, tabagismo e a capacidade de resposta do sistema imunológico. Pacientes com doenças metabólicas, como diabetes e dislipidemias, podem apresentar menor resposta terapêutica, exigindo ajustes na abordagem clínica e no monitoramento da evolução (Gasmi Benahmed et al., 2022).
A resistência antimicrobiana é uma preocupação crescente, especialmente quando antibióticos são utilizados de forma indiscriminada ou sem confirmação da presença de infecção ativa. O uso inadequado pode resultar em falhas terapêuticas, recidivas e efeitos adversos sistêmicos. Por isso, alguns autores defendem que o uso de antibióticos em casos de peri-implantite deve ser restrito a situações específicas, embasadas em evidências microbiológicas e clínicas claras (Rokaya et al., 2020).
Pesquisas recentes vêm explorando a possibilidade de integrar terapias antimicrobianas a abordagens menos invasivas, como a terapia fotodinâmica e a utilização de biomateriais com ação antimicrobiana. Essas tecnologias visam reduzir a carga microbiana de forma mais seletiva, minimizando os impactos colaterais do uso prolongado de antibióticos. Embora ainda em desenvolvimento, essas propostas representam alternativas promissoras para o manejo da peri-implantite, especialmente em pacientes com limitações para o uso de antibióticos sistêmicos (González Regueiro et al., 2021; Herrera et al., 2023).
A análise da resposta terapêutica aos antibióticos requer a utilização de parâmetros objetivos e mensuráveis, o que inclui não apenas a avaliação clínica, mas também o monitoramento de biomarcadores inflamatórios presentes no fluido crevicular peri-implantar. A combinação entre dados clínicos e moleculares permite uma abordagem mais precisa e individualizada, potencializando os benefícios da terapia antimicrobiana e reduzindo o risco de falhas (Hentenaar et al., 2021).
BIOMARCADORES INFLAMATÓRIOS E REGENERATIVOS NA RESPOSTA AO TRATAMENTO DA PERI-IMPLANTITE
O uso de biomarcadores no contexto da peri-implantite tem se destacado como ferramenta complementar ao diagnóstico clínico, permitindo a avaliação da atividade inflamatória e da resposta tecidual ao tratamento. Os biomarcadores são substâncias quantificáveis presentes em fluidos corporais, como o fluido crevicular peri-implantar, que refletem alterações fisiopatológicas locais. Sua identificação pode fornecer subsídios para a personalização da terapia, monitoramento da eficácia do tratamento e predição de desfechos clínicos (Samnam et al., 2024).
Entre os principais biomarcadores estudados na peri-implantite, destacam-se as citocinas inflamatórias, como a interleucina-1β (IL-1β), o fator de necrose tumoral alfa (TNF-α) e a interleucina-6 (IL-6), que participam ativamente da cascata inflamatória e da destruição óssea. Esses marcadores são liberados por células do sistema imune em resposta à presença de patógenos e desempenham papel importante na diferenciação de osteoclastos e na reabsorção do tecido ósseo peri-implantar (Hentenaar et al., 2021).
Além das citocinas, metaloproteinases da matriz (MMPs), como a MMP-8, também são frequentemente avaliadas. Essas enzimas estão envolvidas na degradação da matriz extracelular e são marcadores sensíveis de inflamação ativa. Níveis elevados de MMP-8 no fluido crevicular indicam atividade inflamatória intensa e perda de inserção, sendo úteis tanto no diagnóstico precoce quanto na monitorização da resposta ao tratamento antimicrobiano ou cirúrgico (Samnam et al., 2024).
A avaliação longitudinal dos níveis de biomarcadores permite verificar a resposta biológica às intervenções clínicas. Em estudos com acompanhamento de pacientes tratados com terapias antimicrobianas e cirúrgicas, observou-se redução significativa nos níveis de IL-1β e MMP-8 após o controle da infecção, sugerindo que esses marcadores são sensíveis às variações clínicas e podem indicar remissão ou persistência da doença (Hentenaar et al., 2021; González Regueiro et al., 2021).
Com o avanço das técnicas analíticas, também tem crescido o interesse por biomarcadores relacionados ao metabolismo ósseo, como a osteoprotegerina (OPG) e a proteína relacionada ao receptor ativador do fator nuclear kappa-B ligand (RANKL). A relação entre essas substâncias regula o equilíbrio entre formação e reabsorção óssea. Um aumento da razão RANKL/OPG tem sido associado à progressão da perda óssea peri-implantar, indicando seu valor prognóstico (Rakic et al., 2020).
Outro aspecto investigado é o impacto da carga oclusal e de alterações biomecânicas nos níveis de biomarcadores. Em um estudo com implantes de diâmetro reduzido submetidos à carga funcional, foi observado aumento temporário nos níveis de IL-6 e MMPs, seguido de estabilização após adaptação tecidual, evidenciando a utilidade desses marcadores na identificação de respostas inflamatórias subclínicas (Marcello-Machado et al., 2020).
A personalização da terapia da peri-implantite baseada em biomarcadores requer a integração de dados clínicos e moleculares. Ainda que promissora, essa abordagem enfrenta desafios metodológicos, como a padronização da coleta do fluido crevicular, a variabilidade individual dos níveis basais e a ausência de valores de referência universalmente aceitos. A heterogeneidade dos estudos dificulta a comparação entre resultados e a incorporação desses exames na rotina clínica (Samnam et al., 2024; Hentenaar et al., 2021).
Apesar disso, há consenso na literatura sobre o potencial dos biomarcadores como ferramentas complementares ao exame clínico tradicional. Sua aplicação pode contribuir para diagnósticos mais precoces, especialmente em casos com sinais clínicos pouco evidentes, e para a avaliação objetiva da efetividade terapêutica, evitando tratamentos desnecessários ou excessivos. A monitorização contínua por meio de biomarcadores pode melhorar significativamente a tomada de decisão clínica (Marcello-Machado et al., 2020; González Regueiro et al., 2021).
Biomarcadores também têm sido explorados como indicadores de risco para a peri-implantite em pacientes com doenças sistêmicas ou histórico de periodontite. O perfil inflamatório crônico presente em condições como diabetes, obesidade e dislipidemias parece refletir-se nos níveis aumentados de IL-1β e MMPs no ambiente peri-implantar, o que justifica a necessidade de maior vigilância clínica e intervenções preventivas nesses grupos (Gasmi Benahmed et al., 2022).
O desenvolvimento de painéis multibiomarcadores pode aumentar a precisão diagnóstica e prognóstica. A combinação de diferentes mediadores inflamatórios e ósseos oferece uma visão mais abrangente da atividade da doença, permitindo classificações mais refinadas quanto à gravidade e ao risco de progressão. Essa abordagem integrativa representa um avanço no manejo da peri-implantite, especialmente em um cenário de terapias cada vez mais individualizadas (Samnam et al., 2024).
METODOLOGIA
Este estudo caracteriza-se como uma revisão sistemática de literatura, cujo objetivo é identificar, analisar e sintetizar evidências científicas sobre a eficácia dos antibióticos no tratamento da peri-implantite, com foco na padronização dos protocolos terapêuticos e na aplicação de biomarcadores como instrumentos de monitoramento clínico. A condução da revisão seguiu as recomendações do Preferred Reporting Items for Systematic Reviews and Meta-Analyses (Prisma), garantindo transparência e reprodutibilidade metodológica em todas as etapas.
A questão norteadora da pesquisa foi estruturada com base na estratégia PICO, sendo definidos os seguintes elementos: P (população): pacientes com peri-implantite; I (intervenção): uso de antibióticos; C (comparação): outras intervenções terapêuticas ou ausência de antibióticos; O (desfecho): eficácia clínica, padronização de protocolos e uso de biomarcadores. A pergunta de pesquisa foi: “Qual a eficácia dos antibióticos na peri-implantite e há padronização terapêutica e utilização de biomarcadores na prática clínica?”
A busca bibliográfica foi realizada entre maio e junho de 2025, por meio de acesso eletrônico a bases de dados reconhecidas na área da saúde: PubMed/MEDLINE, Scopus, Web of Science, Embase e Biblioteca Virtual em Saúde (BVS). A estratégia de busca combinou descritores controlados e termos livres em inglês, com operadores booleanos AND e OR, sendo utilizados os seguintes termos: “peri-implantitis”, “antibiotics”, “antimicrobial therapy”, “biomarkers”, “peri-implant crevicular fluid”, “clinical protocols”, “treatment outcomes” e “standardization”. Para garantir abrangência e especificidade, os termos foram adaptados a cada base conforme as exigências do sistema de indexação.
Foram incluídos artigos originais, revisões sistemáticas, estudos clínicos randomizados, séries de casos e estudos de coorte publicados entre 2020 e 2025, em inglês, que abordassem diretamente a eficácia dos antibióticos no tratamento da peri-implantite, bem como a utilização de biomarcadores inflamatórios e regenerativos em sua monitorização. Estudos realizados exclusivamente in vitro, revisões narrativas, artigos com população animal, cartas ao editor e publicações duplicadas foram excluídos da análise.
A síntese dos dados foi realizada de forma descritiva e narrativa, com agrupamento dos estudos por similaridade de abordagem e desfechos. Devido à heterogeneidade metodológica entre os artigos incluídos, não foi realizada meta-análise. Os dados foram confrontados com base na consistência dos resultados, relevância clínica e qualidade metodológica, buscando-se evidenciar padrões, lacunas e contradições nas evidências disponíveis. A apresentação dos resultados foi acompanhada de um fluxograma do processo de seleção dos estudos, conforme os critérios do Prisma.
Este estudo, por se tratar de uma revisão de literatura com dados secundários disponíveis publicamente, não exigiu submissão a Comitê de Ética em Pesquisa, conforme Resolução nº 510/2016 do Conselho Nacional de Saúde.
RESULTADOS E DISCUSSÃO
A presente revisão sistemática identificou, por meio da busca em cinco bases de dados, um total de 102 registros. Após a remoção de 27 duplicatas, restaram 75 estudos para triagem. Nenhum registro foi eliminado antes dessa etapa. A triagem de títulos e resumos resultou na exclusão de 47 publicações que não atendiam aos critérios iniciais. Dos 28 artigos restantes, 20 foram avaliados em texto completo, sendo que 11 deles foram excluídos por apresentarem delineamentos metodológicos inadequados ou por não abordarem diretamente a temática proposta. Ao final do processo, foram incluídos 9 artigos na revisão. O detalhamento do processo de elegibilidade encontra-se representado na Figura 1, conforme diretrizes do Prisma.
Figura 1 – Fluxograma Prisma
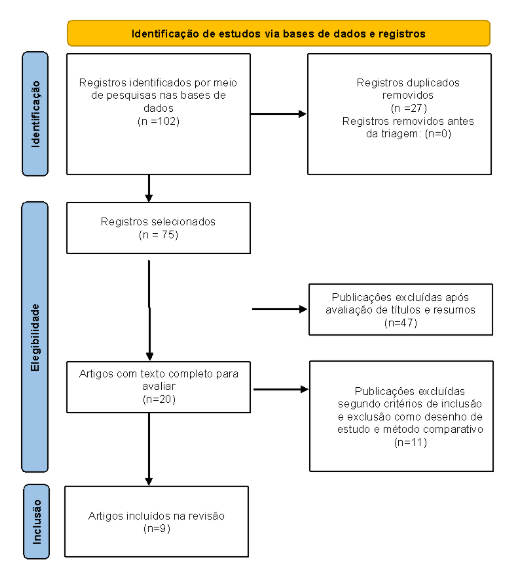
Fonte: Elaborado pelo autor (2025).
Entre os estudos incluídos, observou-se significativa heterogeneidade nos delineamentos e nas abordagens terapêuticas adotadas. O trabalho de González Regueiro et al. (2021) apresentou um estudo de coorte prospectivo que combinou implantoplastia com aplicação local de antibióticos, evidenciando melhora clínica significativa em parâmetros como profundidade de sondagem e sangramento à sondagem. Os autores destacaram que a intervenção cirúrgica aliada ao uso localizado de antimicrobianos promoveu redução da carga bacteriana, sendo uma alternativa viável à terapia exclusivamente mecânica.
Por sua vez, Herrera et al. (2023) desenvolveram uma diretriz clínica de nível S3 baseada em evidências sistemáticas, reunindo estudos sobre prevenção e tratamento das doenças peri-implantares. Embora os autores reconheçam o valor do uso adjuvante de antibióticos, enfatizam que a padronização dos protocolos é inexistente, especialmente no que diz respeito às doses, duração do tratamento e forma de aplicação. A diretriz recomenda cautela na prescrição, sugerindo que o uso de antibióticos sistêmicos deve ser restrito a casos avançados e sempre associado à intervenção mecânica ou cirúrgica.
Rokaya et al. (2020), em revisão abrangente sobre peri-implantite, reforçam que a terapêutica baseada apenas em antibióticos, sem controle mecânico adequado do biofilme, é ineficaz. O artigo alerta para a resistência antimicrobiana e recomenda a aplicação local de agentes antimicrobianos como estratégia de menor risco. Destaca-se, ainda, que o sucesso clínico depende da resposta imunológica do paciente, da condição sistêmica e da técnica cirúrgica adotada, elementos pouco padronizados nos estudos.
No estudo conduzido por Hentenaar et al. (2021), os níveis de biomarcadores inflamatórios no fluido crevicular peri-implantar foram analisados em três grupos: implantes saudáveis, com peri-implantite sem tratamento e com peri-implantite tratados sem cirurgia. Os resultados evidenciaram diferenças significativas nos níveis de interleucina-1β e metaloproteinase-8, sugerindo que esses marcadores são úteis para monitoramento da atividade inflamatória. O estudo indica que intervenções clínicas que incluem antibióticos estão associadas à redução desses marcadores.
A pesquisa de Marcello-Machado et al. (2020) observou os efeitos da carga oclusal sobre implantes de diâmetro reduzido, avaliando biomarcadores antes e após a instalação protética. Apesar de não investigar diretamente o uso de antibióticos, os dados demonstram que alterações biomecânicas afetam os níveis de citocinas inflamatórias, o que pode influenciar a resposta ao tratamento da peri-implantite, especialmente em situações clínicas onde a biomecânica não é devidamente controlada.
O estudo de Samnam et al. (2024) realizou uma revisão integrativa sobre biomarcadores no fluido crevicular, destacando seu potencial para diagnóstico precoce e avaliação prognóstica. Os autores indicam que a combinação de biomarcadores inflamatórios e de remodelação óssea, como RANKL e OPG, pode contribuir para personalização terapêutica. Em relação aos antibióticos, o estudo reforça que a resposta inflamatória pode ser monitorada com maior precisão mediante quantificação desses mediadores, o que favorece ajustes terapêuticos mais assertivos.
Gasmi Benahmed et al. (2022) investigaram a influência de condições metabólicas na evolução da peri-implantite, com ênfase em pacientes com diabetes e dislipidemias. Os achados sugerem que esses indivíduos apresentam perfis inflamatórios mais exacerbados, com níveis elevados de citocinas pró-inflamatórias. Assim, os antibióticos podem ter eficácia reduzida em pacientes com desregulação sistêmica, sendo necessária uma abordagem mais integrada que envolva controle metabólico e terapias adjuvantes.
Cui et al. (2025) realizaram revisão sobre a disbiose microbiana e a resposta imune em peri-implantite. O estudo reforça que, embora os antibióticos possam temporariamente controlar a carga bacteriana, a modulação da resposta inflamatória depende do restabelecimento do equilíbrio ecológico local. Os autores recomendam a combinação entre terapias antimicrobianas e técnicas de modulação imunológica para controle duradouro da doença.
Por fim, Atieh et al. (2020) exploraram a etiologia da peri-implantite sob uma perspectiva integrada, relacionando fatores microbianos, anatômicos e sistêmicos. Embora não realizem experimentação clínica direta, os autores sintetizam que o êxito terapêutico depende de uma abordagem personalizada, onde antibióticos devem ser indicados com base no risco individual, na extensão da infecção e na capacidade de resposta do paciente.
Ao confrontar os estudos, nota-se convergência em relação à inexistência de padronização terapêutica para o uso de antibióticos no tratamento da peri-implantite. Embora todos reconheçam os benefícios da intervenção antimicrobiana como adjuvante, não há consenso quanto às melhores práticas, doses ou tipos de antibióticos. Herrera et al. (2023), Rokaya et al. (2020) e González Regueiro et al. (2021) convergem quanto à necessidade de integração com terapias mecânicas e cirúrgicas, enquanto Gasmi Benahmed et al. (2022) e Cui et al. (2025) chamam atenção para fatores sistêmicos e imunológicos que impactam diretamente a eficácia dos tratamentos.
No que se refere aos biomarcadores, a literatura analisada demonstra amplo consenso sobre sua aplicabilidade clínica, tanto para diagnóstico precoce quanto para acompanhamento terapêutico. Hentenaar et al. (2021), Samnam et al. (2024) e Marcello-Machado et al. (2020) apresentam evidências de que mediadores como IL-1β, MMP-8, RANKL e OPG são sensíveis a variações inflamatórias locais e podem orientar a conduta clínica de forma mais precisa. Contudo, apontam a necessidade de padronização dos métodos de coleta e interpretação dos resultados, o que ainda limita sua incorporação rotineira.
Em síntese, os resultados revelam que, embora os antibióticos desempenhem papel relevante no controle da peri-implantite, seu uso ainda carece de protocolos uniformes e deve ser contextualizado às condições individuais do paciente. A adoção de biomarcadores como suporte diagnóstico e prognóstico representa um avanço promissor, desde que validada por metodologias clínicas padronizadas e incorporada de forma integrada à avaliação clínica tradicional.
CONSIDERAÇÕES FINAIS
A análise sistemática da literatura permitiu identificar que a utilização de antibióticos no tratamento da peri-implantite apresenta eficácia clínica variável, especialmente quando empregados como adjuvantes a terapias mecânicas ou cirúrgicas. Observou-se ausência de padronização quanto ao tipo, via de administração, posologia e tempo de uso dos antimicrobianos, o que dificulta a comparação entre estudos e compromete a reprodutibilidade dos resultados. Além disso, a presença de fatores sistêmicos, como doenças metabólicas e condições imunológicas específicas, influencia significativamente a resposta ao tratamento, exigindo abordagens individualizadas.
No que se refere aos biomarcadores inflamatórios e regenerativos, constatou-se que substâncias como interleucinas, metaloproteinases e proteínas reguladoras da atividade óssea representam ferramentas promissoras para o monitoramento da atividade da doença e da resposta terapêutica. Contudo, a utilização clínica desses marcadores ainda enfrenta limitações metodológicas, como a falta de protocolos padronizados para coleta, análise e interpretação dos dados.
Diante disso, destaca-se a importância de aprofundar as investigações sobre o uso racional de antibióticos na peri-implantite, priorizando estudos com delineamentos robustos, maior controle de variáveis e foco na integração de parâmetros clínicos e moleculares. A incorporação de biomarcadores ao protocolo clínico poderá representar um avanço no manejo personalizado da doença, desde que sustentada por evidências consistentes e reprodutíveis. Em suma, a prática clínica baseada em evidências e ajustada ao perfil individual do paciente constitui o caminho mais seguro e eficaz para o enfrentamento da peri-implantite.
REFERÊNCIAS BIBLIOGRÁFICAS
AL-KHUREIF, A. A. et al. Clinical, host-derived immune biomarkers and microbiological outcomes with adjunctive photochemotherapy compared with local antimicrobial therapy in the treatment of peri-implantitis in cigarette smokers. Photodiagnosis and Photodynamic Therapy, v. 30, p. 101684, 2020. Disponível em: https://www.sciencedirect.com/science/article/pii/S1572100020300375. Acesso em: 15 maio 2025.
ATIEH, M. A.; SHAH, M.; ALSABEEHA, N. H. M. Etiology of peri-implantitis. Current Oral Health Reports, v. 7, p. 313-320, 2020. Disponível em: https://link.springer.com/article/10.1007/s40496-020-00276-0. Acesso em: 21 maio 2025.
BLANCO, C. et al. Peri-implantitis, systemic inflammation, and dyslipidemia: a cross-sectional biochemical study. Journal of Periodontal & Implant Science, v. 51, n. 5, p. 342, 2021. Disponível em: https://pmc.ncbi.nlm.nih.gov/articles/PMC8558006/pdf/jpis-51-342.pdf. Acesso em: 19 maio 2025.
CUI, Z.; WANG, P.; GAO, W. Microbial dysbiosis in periodontitis and peri-implantitis: pathogenesis, immune responses, and therapeutic. Frontiers in Cellular and Infection Microbiology, v. 15, p. 1517154, 2025. Disponível em: https://www.frontiersin.org/journals/cellular-and-infection-microbiology/articles/10.3389/fcimb.2025.1517154/pdf. Acesso em: 12 maio 2025.
GASMI BENAHMED, A. et al. Metabolic conditions and peri-implantitis. Antibiotics, v. 12, n. 1, p. 65, 2022. Disponível em: https://www.mdpi.com/2079-6382/12/1/65. Acesso em: 15 maio 2025.
GONZÁLEZ REGUEIRO, I. et al. Surgical approach combining implantoplasty and reconstructive therapy with locally delivered antibiotic in the treatment of peri‐implantitis: A prospective clinical case series. Clinical Implant Dentistry and Related Research, v. 23, n. 6, p. 864-873, 2021. Disponível em: https://onlinelibrary.wiley.com/doi/pdfdirect/10.1111/cid.13049. Acesso em: 27 maio. 2025.
GUL, S. S. et al. Diagnostic accuracy of oral fluids biomarker profile to determine the current and future status of periodontal and peri-implant diseases. Diagnostics, v. 10, n. 10, p. 838, 2020. Disponível em: https://www.mdpi.com/2075-4418/10/10/838. Acesso em: 10 maio 2025.
HENTENAAR, D. F. M. et al. Biomarker levels in peri‐implant crevicular fluid of healthy implants, untreated and non‐surgically treated implants with peri‐implantitis. Journal of Clinical Periodontology, v. 48, n. 4, p. 590-601, 2021. Disponível em: https://research.rug.nl/files/164265680/jcpe.13423.pdf. Acesso em: 22 maio 2025.
HERRERA, D. et al. Prevention and treatment of peri‐implant diseases—The EFP S3 level clinical practice guideline. Journal of Clinical Periodontology, v. 50, p. 4-76, 2023. Disponível em: https://onlinelibrary.wiley.com/doi/pdfdirect/10.1111/jcpe.13823. Acesso em: 19 maio 2025.
MARCELLO-MACHADO, R. M. et al. Mapping of inflammatory biomarkers in the peri-implant crevicular fluid before and after the occlusal loading of narrow diameter implants. Clinical Oral Investigations, v. 24, p. 1311-1320, 2020. Disponível em: https://link.springer.com/article/10.1007/s00784-019-03010-y. Acesso em: 21 maio 2025.
RAKIC, M. et al. Is the personalized approach the key to improve clinical diagnosis of peri‐implant conditions? The role of bone markers. Journal of Periodontology, v. 91, n. 7, p. 859-869, 2020. Disponível em: https://rfos.fon.bg.ac.rs/bitstream/handle/123456789/2547/AccIsthePersonalized.pdf?sequence=1. Acesso em: 13 maio 2025.
ROKAYA, D. et al. Peri-implantitis update: risk indicators, diagnosis, and treatment. European Journal of Dentistry, v. 14, n. 4, p. 672-682, 2020. Disponível em: https://www.thieme-connect.com/products/ejournals/pdf/10.1055/s-0040-1715779.pdf. Acesso em: 28 maio 2025.
SAMNAM, N. et al. Biomarkers in peri-implant crevicular fluid: insights into diagnosis and prognosis of peri-implant diseases. Frontiers in Health Informatics, v. 13, n. 8, 2024. Disponível em: https://www.mdpi.com/2075-4418/10/10/838. Acesso em: 15 maio 2025.
Referencias
Share this :
Área do Conhecimento









