Câncer bucal – O papel do palmitato e estearato na inibição da via CGAS-STING-IFN-1
ORAL CANCER - THE ROLE OF PALMITATE AND STEARATE IN INHIBITING THE CGAS-STING-IFN-1 PATHWAY
CÁNCER ORAL - EL PAPEL DEL PALMITATO Y EL ESTEARATO EN LA INHIBICIÓN DE LA VÍA CGAS-STING-IFN-1
Autor
URL do Artigo
https://iiscientific.com/artigos/E5376B
DOI
doi.org/10.63391/E5376B
Resumo
Summary
Resumen
INTRODUÇÃO
O câncer bucal representa uma das principais neoplasias malignas da região de cabeça e pescoço (Inca, 2023; Who, 2022). Além dos fatores clássicos de risco como tabaco, álcool, exposição solar e infecção por HPV, os fatores dietéticos vêm ganhando cada vez mais espaço na literatura científica, por sua predisposição na tumorigênese oral.
O quadro a seguir (Quadro 1) apresenta as estimativas de novos casos e mortes causadas por tumores bucais no mundo, nos anos de 2022 e 2025, segundo a International Agency for Research on Cancer (Novisk et al., 2025).
Quadro 1 – Números de novos casos e mortes por câncer bucal no mundo
![]()
2022 2025
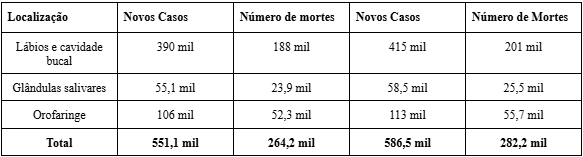
Fonte: Novisk et al., 2025
O consumo elevado de alimentos ultraprocessados, ricos em ácidos graxos saturados (AGS) como palmitato e estearato, tem sido associado a processos inflamatórios crônicos, disfunção mitocondrial, alterações epigenéticas e supressão imune (Siri-Tarino et al., 2010; De Souza et al., 2015; Meng et al., 2021). Esses compostos, oriundos principalmente da gordura de palma (palmitato) e de fontes animais e vegetais (estearato), são amplamente empregados como emulsificantes e estabilizantes na indústria de alimentos processados, farmacêutica e cosmética (CIR, 2018).
Heath et al. (2023), demonstraram que o palmitato atua como regulador negativo da via STING (Stimulator of Interferon Genes) ao interferir na ativação da cGAS (cyclic GMP-AMP synthase), reduzindo a produção de IFN-1 (Interferon tipo 1) e favorecendo um ambiente imunossupressor que contribui para a evasão tumoral. Esse processo é particularmente relevante na carcinogênese bucal, onde a resposta imune local desempenha papel fundamental no controle da proliferação celular anormal e na supressão tumoral. Essa interferência do palmitato compromete a sinalização inflamatória benéfica que recruta células T citotóxicas e outras células efetoras da imunidade inata e adaptativa (Zhu et al., 2019).
Além da inibição da via STING, os AGS também afetam outras vias de sinalização, como TLR4 (Receptor Toll-like 4) e mTOR (mammalian Target of Rapamycin), que influenciam diretamente o equilíbrio entre imunidade protetora e inflamação crônica. Esses efeitos são agravados por fatores como obesidade e resistência à insulina, frequentemente presentes em dietas ricas em alimentos ultraprocessados (Wang et al., 2023).
Os TLRs regulam inúmeras respostas biológicas, incluindo as respostas imunes e inflamatórias durante a carcinogênese. Os TLRs podem promover a tumorigênese por meio de sinais inflamatórios promotores de tumores, vias antiapoptóticas, mecanismos de proliferação celular e ativação de fibroblastos, influenciando células tumorais ou o microambiente tumoral. A associação dos TLRs no OSCC é controversa. Contudo, muitos estudos demonstraram um papel do TLR4 na patogênese do câncer (Rusanen et al., 2024).
A via PI3K/AKT/mTOR (fosfoinositídeo 3-quinase/proteína quinase B/mammalian Target of Rapamycin) regula o crescimento, metabolismo e sobrevivência celular. Em carcinomas escamosos orais, essa via é frequentemente hiperativada, contribuindo para a proliferação tumoral acelerada, resistência à radioterapia e adaptação metabólica, com expressão elevada de p‑mTOR associada a pior sobrevida e maiores taxas de recidiva (Jiang et al., 2024).
A substituição de aditivos derivados de ácidos graxos saturados, como sais e ésteres de palmitato e estearato, por alternativas menos nocivas, tem se mostrado uma tendência crescente na indústria alimentícia, impulsionada pela busca por segurança, funcionalidade e menor resultado inflamatório. Torna-se cada vez mais necessário aprofundar o conhecimento e a compreensão sobre os fatores dietéticos e ambientais envolvidos na fisiopatologia do câncer bucal. As pesquisas são claras acerca de que não basta ser natural ou vegano para ser saudável e não comprometer as vias metabólicas.
METODOLOGIA
Este estudo consiste em uma revisão integrativa da literatura, realizada nas bases PubMed, Web of Science, Scopus e SciELO. Os descritores utilizados foram: “oral cancer”, “palmitic acid”, “stearic acid”, “STING pathway”, “IFN-1”, “saturated fatty acids”, “natural emulsifiers” e “diet and cancer”. Foram incluídos artigos entre 2015 e 2025, em língua portuguesa e inglesa.
Os critérios de inclusão abrangeram estudos com modelo experimental (in vitro e in vivo), revisões sistemáticas, ensaios clínicos e artigos originais relacionados ao câncer bucal e/ou vias de resposta imune moduladas por ácidos graxos saturados.
RESULTADOS E DISCUSSÃO
A interação dos AGS com as vias moleculares de defesa celular, como a via cGAS-STING-IFN-1, pode comprometer a imunovigilância tumoral e favorecer a evasão imune de células neoplásicas (Heath et al., 2023). A via cGAS-STING-IFN-1 é uma importante rota de detecção de DNA citosólico, que inicia uma resposta imune inata protetora contra patógenos e células tumorais. A enzima cGAS (cyclic GMP-AMP synthase) reconhece o DNA fora do núcleo celular e ativa a proteína STING, culminando na produção de IFN-1, que desempenha papel central na imunovigilância tumoral (Chen; Sun; Chen, 2016).
Heath et al. (2023), demonstraram que os AGS suprimem a imunogenicidade tumoral, ao inibir a via STING via NLRC3 (NOD-like receptor family CARD domain containing 3), proteína envolvida na modulação da resposta imune. Esse inibidor interage com STING, bloqueando a cascata de ativação do IFN-1 (interferon tipo 1). Estudos destacam o papel do NLRC3 como um inibidor natural da via cGAS-STING. Essa proteína atua negativamente sobre a translocação da STING, bloqueando a produção de IFN-1 e reduzindo a resposta imune inata. A superexpressão de NLRC3 tem sido associada à evasão tumoral e à imunossupressão no microambiente neoplásico (Zhu et al., 2019; Chen; Sun; Chen, 2016). Essa inibição pode contribuir para o desenvolvimento do câncer bucal com a menor ativação de linfócitos citotóxicos e redução da destruição de células tumorais, agravando o quadro imunológico local. A interação entre fatores dietéticos, como o consumo excessivo de AGS, e mecanismos inibitórios moleculares como o NLRC3, reforça a importância de estratégias preventivas baseadas em alimentação saudável (Heath et al., 2023; Zhu et al., 2019; Chen; Sun; Chen, 2016; De Souza et al., 2015).
A via cGAS-STING tem papel fundamental na resposta imune inata, sendo ativada na presença de DNA citosólico, promovendo a expressão de interferons tipo I. Esses, por sua vez, ativam linfócitos citotóxicos e a destruição de células tumorais. A inibição dessa via por AGS, como demonstrado por Heath et al. (2023), representa um importante mecanismo de imunoedição tumoral.
O palmitato, ou ácido palmítico, é um dos AGS mais prevalentes na dieta ocidental, podendo ser sintetizado endogenamente a partir de carboidratos, mas também é ingerido em grande quantidade quando do consumo de alimentos industrializados. O estearato, ou ácido esteárico, também tem demonstrado impacto na função mitocondrial e na resposta inflamatória em modelos experimentais (Cir, 2018; Efsa, 2020).
A exposição crônica a ácidos graxos saturados, como o palmitato e o estearato, também influencia negativamente a sinalização de vias celulares envolvidas na regulação da imunidade e do metabolismo tumoral. A ativação persistente do receptor TLR4, associados à necrose tumoral ou inflamação induzida por AGS, favorece um ambiente pró-inflamatório, recrutando células mielóides imaturas e promovendo imunossupressão (Yang et al., 2024). Essa ativação desregulada do TLR4 em células epiteliais orais tem sido associada à progressão do carcinoma espinocelular bucal e à resistência da terapia (Mohan et al., 2023). Paralelamente, os AGS ativam a via PI3K/AKT/mTOR, que regula o crescimento celular e o metabolismo energético. A hiperativação de mTOR, observada em amostras de OSCC, está relacionada a uma maior agressividade tumoral, ao aumento da proliferação e inibição da autofagia, favorecendo a adaptação tumoral ao microambiente (Wang et al., 2023). A interação entre TLR4, mTOR, cGAS-STING e proteínas inibitórias como NLRC3 reforça o papel central dos fatores dietéticos na modulação do microambiente tumoral oral, destacando a importância de intervenções alimentares na prevenção do câncer bucal.
TLR4 é um receptor que reconhece padrões moleculares derivados de microrganismos ou células danificadas, e ativa vias de sinalização importantes no sistema imune inato. Estudos mostram que a superexpressão de TLR4 em OSCC está associada a pior prognóstico, invasão tumoral e microambiente inflamatório crônico, favorecendo a progressão e evasão imune (Rusanen et al., 2024).
Pesquisas indicam que dietas ricas em palmitato e estearato modulam negativamente a via STING, comprometendo a produção de IFN-1 e a resposta antitumoral. Estudos em camundongos obesos e em culturas celulares de carcinomas escamosos evidenciaram aumento da carga tumoral, redução de linfócitos T efetores e evasão imune (Heath et al., 2023; Lei et al., 2022).
Estudos experimentais reforçam que o ácido palmítico compromete a ativação da proteína cGAS e diminui a secreção de IFN-1, reduzindo a capacidade de células sintetizadoras de antígenos em promover resposta antitumoral (Heath et al., 2023; Zhu et al., 2019). Já o ácido esteárico tem demonstrado modulação negativa na função mitocondrial e aumento da resistência tumoral em modelos animais (Meng et al., 2021).
A substituição de aditivos derivados de ácidos graxos saturados, como sais e ésteres de palmitato e estearato por alternativas que demonstram menor nocividade tem se mostrado uma tendência crescente na indústria alimentícia, impulsionada pela busca por segurança, funcionalidade e menor impacto inflamatório (Choi et al., 2015; Maarek et al., 2019). O Quadro 2 apresenta os principais substitutos naturais ao palmitato e estearato, com destaque para sua origem, função e benefícios nutricionais.
Quadro 2 – Substituições sugeridas ao palmitato e estearato em alimentos industrializados
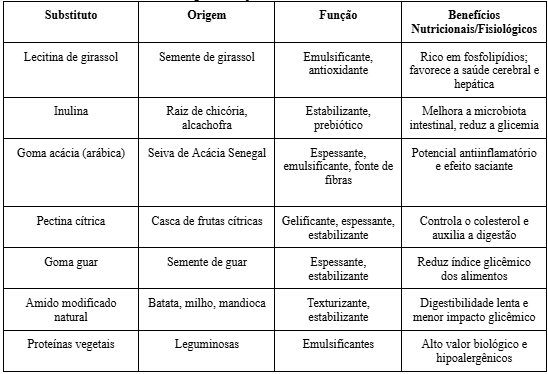
Fonte: Choi, Y. H. et al., 2015; Viuda- Martos, M. et al., 2015; Efsa, 2017; Maarek, A. et al., 2019; FAO/WHO, 2021; MDPI, 2021; US FDA, 2020–2024.
O uso de aditivos como o estearato de magnésio pode afetar negativamente a biodisponibilidade de micronutrientes e não apresenta função nutricional positiva. Em contrapartida, emulsificantes naturais como lecitina de girassol, goma arábica, inulina e glicerídeos vegetais têm demonstrado menor impacto inflamatório e boa aplicação tecnológica (MDPI, 2021).
CONSIDERAÇÕES FINAIS
Diante das evidências analisadas, é possível concluir que o palmitato e o estearato, frequentemente utilizados como aditivos alimentares em alimentos ultraprocessados, podem desempenhar papel relevante na modulação negativa da imunidade antitumoral, especialmente por meio da interferência na via cGAS-STING e na produção de interferons do tipo 1. Esses componentes lipídicos saturados têm papel significativo na inibição de vias imunes, fundamentais na defesa antitumoral. Tais compostos, amplamente presentes na indústria alimentícia, devem ser reavaliados quanto à sua segurança metabólica e imunológica. A substituição por óleos vegetais insaturados e emulsificantes naturais é altamente recomendável, não apenas pela segurança funcional, mas por seus efeitos benéficos no sistema imune. Essa mudança também deve ser contemplada em políticas de saúde e programas de educação alimentar e nutricional.
A compreensão da relação entre dieta e imunidade tem se mostrado essencial no enfrentamento de doenças como o câncer bucal, cuja prevenção vai além do combate ao tabaco e ao álcool. A reformulação de alimentos com ingredientes naturais e com menor potencial inflamatório surge como uma estratégia promissora na promoção da saúde e na redução de fatores de risco associados ao desenvolvimento de neoplasias orais. O incentivo à pesquisa, à educação alimentar e à regulamentação mais rigorosa dos aditivos utilizados em larga escala pela indústria são caminhos importantes para a construção de uma abordagem preventiva mais ampla e eficaz no combate ao câncer bucal.
REFERÊNCIAS BIBLIOGRÁFICAS
CHAFFEE, B. W.; WATKINS, S. L.; GLANTZ, S. A. Electronic Cigarettes and Oral Health: A Review of the Literature. Journal of the American Dental Association, v. 147, n. 7, p. 510–518, 2016. DOI: 10.1016/j.adaj.2016.03.006.
CHEN, Q.; SUN, L.; CHEN, Z. J. Regulation and function of the cGAS–STING pathway of cytosolic DNA sensing. Nature Immunology, v. 17, p. 1142–1149, 2016. DOI: https://doi.org/10.1038/ni.3558.
CHOI, Y. H. et al. Inulin-type fructans and immune modulation. Journal of Nutrition & Biochemistry, v. 26, p. 923–932, 2015.
CIR – Cosmetic Ingredient Review. Final Report on the Safety Assessment of Stearic Acid, Oleic Acid, Palmitic Acid, Myristic Acid, and Related Ingredients. International Journal of Toxicology, v. 27, p. 1–82, 2018.
DE SOUZA, R. J. et al. Saturated and trans fats and the risk of all-cause mortality, cardiovascular disease, and type 2 diabetes. BMJ, v. 351, 2015. DOI: 10.1136/bmj.h3978.
EFSA – EUROPEAN FOOD SAFETY AUTHORITY. Re-evaluation of lecithins (E 322) as a food additive. EFSA Journal, v. 15, n. 4, 2017.
FAO/WHO. Food additives – Specifications and evaluations. Joint FAO/WHO Expert Committee on Food Additives (JECFA), 2021.
HEATH, B. R. et al. Saturated fatty acids dampen the immunogenicity of cancer by suppressing STING. Cell Reports, v. 42, n. 4, 2023. DOI: https://doi.org/10.1016/j.celrep.2023.112303.
INCA – Instituto Nacional de Câncer. Estimativa 2023: Incidência de câncer no Brasil. Rio de Janeiro: INCA, 2023.
Jiang Q, Xiao J, Hsieh Y-C, Kumar NL, Han L, Zou Y, Li H. The Role of the PI3K/Akt/mTOR Axis in Head and Neck Squamous Cell Carcinoma. Biomedicines. 2024; 12(7):1610. https://doi.org/10.3390/biomedicines12071610
MAAREK, A. et al. Natural gums and emulsifiers in food. Food Hydrocolloids, v. 86, p. 209–221, 2019.
MDPI – International Journal of Molecular Sciences. Natural emulsifiers and their roles in food safety. IJMS, v. 22, n. 4, p. 2142, 2021. DOI: https://doi.org/10.3390/ijms22042142.
MENG, X. et al. Stearic acid promotes tumor progression by enhancing mitochondrial fusion and metabolism in colorectal cancer cells. Journal of Experimental & Clinical Cancer Research, v. 40, n. 1, 2021, p. 69. DOI: https://doi.org/10.1186/s13046-021-01872-6.
MOHAN, S. et al. TLR4 overexpression promotes tumor progression and immune evasion in oral squamous cell carcinoma. PLOS ONE, v. 19, n. 1, 2023. DOI: 10.1371/journal.pone.0300437.
NOVISK, L. C. et al. Electronic cigarettes: risk of developing oral cancer or an alternative to help in quitting smoking? Aracê, v. 7, n. 7, p. 37056–37082, 2025. DOI: 10.56238/arev7n7-106. Disponível em: https://periodicos.newsciencepubl.com/arace/article/view/6477.
Rusanen P, Marttila E, Amatya SB, Hagström J, Uittamo J, Reunanen J, et al. (2024) Expression of Toll-like receptors in oral squamous cell carcinoma. PLoS ONE 19(4): e0300437. https://doi.org/10.1371/journal.pone.0300437
SIRI-TARINO, P. W. et al. Meta-analysis of prospective cohort studies evaluating the association of saturated fat with cardiovascular disease. American Journal of Clinical Nutrition, v. 91, n. 3, p. 535–546, 2010.
U.S. FOOD AND DRUG ADMINISTRATION – FDA. GRAS Notices (Generally Recognized As Safe), 2020–2024.
YANG, W. et al. Saturated fatty acids promote chronic inflammation via TLR4-mediated macrophage polarization. Journal of Immunology Research, v. 2024, Art. ID 4628375, 2024. DOI: 10.1155/2024/4628375.
WANG, L. et al. Role of mTOR pathway in oral squamous cell carcinoma and its potential as therapeutic target. Biomedicines, v. 12, n. 7, 2023, p. 1610. DOI: 10.3390/biomedicines12071610.
WHO – World Health Organization. Oral cancer: prevention and control. Geneva: WHO, 2022.
ZHU, H. et al. The STING pathway: a double-edged sword in cancer immunity and therapeutics. Nature Reviews Drug Discovery, v. 18, n. 6, 2019, p. 433–452. DOI: https://doi.org/10.1038/s41573-019-0011-1.
Referencias
Share this :
Área do Conhecimento









